-
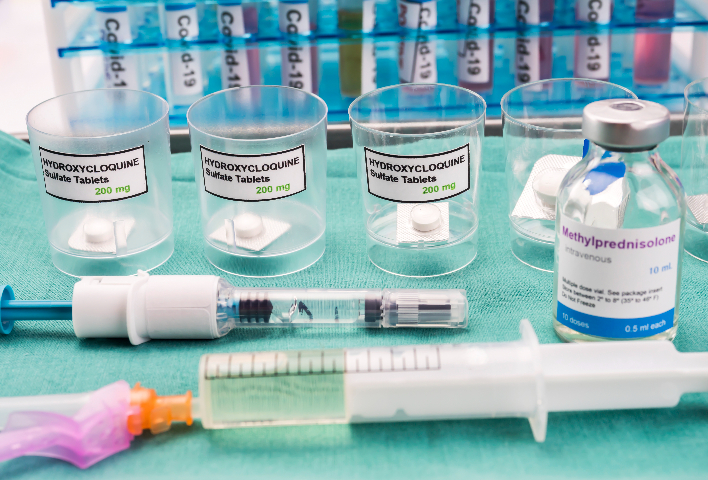 昆山生物試劑出口報(bào)關(guān)
昆山生物試劑出口報(bào)關(guān)進(jìn)口生物試劑的企業(yè)必須具備特定資質(zhì)。首先,企業(yè)需完成對(duì)外貿(mào)易經(jīng)營(yíng)者備案登記,獲得合法進(jìn)出口經(jīng)營(yíng)權(quán)。若進(jìn)口藥品類(lèi)生物試劑,應(yīng)持有有效的藥品經(jīng)營(yíng)許可證,其倉(cāng)儲(chǔ)、運(yùn)輸?shù)仍O(shè)施要符合藥品經(jīng)營(yíng)質(zhì)量管理規(guī)范(GSP),確保試劑儲(chǔ)存與流通環(huán)節(jié)質(zhì)量可控。對(duì)于醫(yī)療器械類(lèi)生物試劑進(jìn)口,企業(yè)需依據(jù)試劑風(fēng)險(xiǎn)等級(jí),完成醫(yī)療器械經(jīng)營(yíng)備案或取得醫(yī)療器械經(jīng)營(yíng)許可證。企業(yè)還應(yīng)配備專(zhuān)業(yè)人員,包括熟悉生物試劑法規(guī)、質(zhì)量控制及進(jìn)口業(yè)務(wù)流程的管理人員與技術(shù)人員,以滿(mǎn)足進(jìn)口業(yè)務(wù)的專(zhuān)業(yè)操作與合規(guī)管理需求。生物試劑進(jìn)口需關(guān)注目的國(guó)對(duì)生物試劑行業(yè)的扶持政策。昆山生物試劑出口報(bào)關(guān)進(jìn)出口的生物試劑必須符合目標(biāo)市場(chǎng)的質(zhì)量與安全標(biāo)準(zhǔn)。在出口環(huán)節(jié),產(chǎn)品要...
2025-04-26 -
 無(wú)錫酶類(lèi)試劑進(jìn)出口審批單代辦
無(wú)錫酶類(lèi)試劑進(jìn)出口審批單代辦隨著全球經(jīng)濟(jì)格局變化,生物試劑進(jìn)出口在新興市場(chǎng)涌現(xiàn)諸多機(jī)遇。東南亞地區(qū),經(jīng)濟(jì)快速發(fā)展,醫(yī)療衛(wèi)生和科研投入不斷增加。以印度尼西亞為例,有關(guān)部門(mén)大力推動(dòng)醫(yī)療基礎(chǔ)設(shè)施建設(shè),對(duì)診斷試劑、科研用生物試劑需求持續(xù)上升。非洲大陸在疾病防控和生物醫(yī)學(xué)研究方面的重視程度日益提高,對(duì)各類(lèi)生物試劑需求呈現(xiàn)爆發(fā)式增長(zhǎng)。當(dāng)?shù)貙?duì)傳染病診斷試劑、疫苗研發(fā)用生物試劑需求迫切,為生物試劑進(jìn)出口企業(yè)開(kāi)辟了廣闊市場(chǎng)空間。拉丁美洲的巴西、阿根廷等國(guó)家,在農(nóng)業(yè)生物技術(shù)、生物醫(yī)藥領(lǐng)域發(fā)展迅速,對(duì)農(nóng)業(yè)生物試劑、不錯(cuò)生物醫(yī)藥研發(fā)試劑需求旺盛。企業(yè)若能提前布局新興市場(chǎng),精細(xì)對(duì)接當(dāng)?shù)匦枨螅型谏镌噭┻M(jìn)出口領(lǐng)域開(kāi)拓新的業(yè)務(wù)增長(zhǎng)點(diǎn)。生物試劑進(jìn)口...
2025-04-25 -
 杭州生物試劑出口審批備案代辦
杭州生物試劑出口審批備案代辦全球生物試劑市場(chǎng)規(guī)模龐大且持續(xù)增長(zhǎng)。在科研領(lǐng)域,生命科學(xué)研究不斷深入,對(duì)生物試劑需求日益旺盛,推動(dòng)市場(chǎng)擴(kuò)張。歐美地區(qū)科研投入高,是主要消費(fèi)市場(chǎng),擁有眾多有名生物試劑企業(yè),技術(shù)先進(jìn)、產(chǎn)品線(xiàn)豐富。亞洲地區(qū),隨著經(jīng)濟(jì)發(fā)展和科研實(shí)力提升,特別是中國(guó)、印度等國(guó)家,市場(chǎng)潛力巨大,需求增速高于全球平均水平。從產(chǎn)品類(lèi)型看,分子生物學(xué)試劑、免疫診斷試劑等細(xì)分市場(chǎng)占據(jù)較大份額。在進(jìn)出口貿(mào)易中,發(fā)達(dá)國(guó)家多為不錯(cuò)生物試劑出口國(guó),憑借技術(shù)優(yōu)勢(shì)把控重心產(chǎn)品供應(yīng);發(fā)展中國(guó)家在中低端產(chǎn)品領(lǐng)域有一定競(jìng)爭(zhēng)力,同時(shí)也是不錯(cuò)試劑重要進(jìn)口市場(chǎng)。企業(yè)需結(jié)合市場(chǎng)趨勢(shì),找準(zhǔn)定位,制定合適進(jìn)出口策略,開(kāi)拓市場(chǎng)份額。出口生物試劑選擇物流時(shí),要考...
2025-04-25 -
 上海特殊物品進(jìn)口報(bào)關(guān)
上海特殊物品進(jìn)口報(bào)關(guān)生物試劑進(jìn)出口需歷經(jīng)復(fù)雜的認(rèn)證流程。在國(guó)內(nèi),生產(chǎn)企業(yè)若想出口生物試劑,首先要通過(guò)國(guó)內(nèi)相關(guān)部門(mén)的生產(chǎn)許可認(rèn)證,例如遵循《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》,滿(mǎn)足生產(chǎn)場(chǎng)地、設(shè)備、人員資質(zhì)等一系列要求,獲得醫(yī)療器械生產(chǎn)許可證。針對(duì)出口產(chǎn)品,還需取得目標(biāo)市場(chǎng)的認(rèn)證,像歐盟的 CE 認(rèn)證,需按照其指令和協(xié)調(diào)標(biāo)準(zhǔn),完成產(chǎn)品測(cè)試、技術(shù)文件編制以及公告機(jī)構(gòu)審核等步驟,證明產(chǎn)品符合歐洲安全、健康和環(huán)保標(biāo)準(zhǔn)。美國(guó)市場(chǎng)則要求企業(yè)通過(guò) FDA 的相關(guān)認(rèn)證,涵蓋產(chǎn)品注冊(cè)、工廠檢查等環(huán)節(jié)。進(jìn)口生物試劑到國(guó)內(nèi)時(shí),同樣要依據(jù)國(guó)內(nèi)法規(guī)完成注冊(cè)備案,如藥品類(lèi)生物試劑要在國(guó)家藥品監(jiān)督管理局進(jìn)行進(jìn)口藥品注冊(cè)申請(qǐng),只有成功完成各項(xiàng)認(rèn)證流程,生...
2025-04-24 -
 無(wú)錫免疫診斷試劑進(jìn)出口檢驗(yàn)檢疫
無(wú)錫免疫診斷試劑進(jìn)出口檢驗(yàn)檢疫若生物試劑含有毒有害物質(zhì),進(jìn)口前需通過(guò)環(huán)保部門(mén)的審批。企業(yè)要向當(dāng)?shù)厣鷳B(tài)環(huán)境部門(mén)提交進(jìn)口申請(qǐng),說(shuō)明生物試劑所含毒有害物質(zhì)的種類(lèi)、含量、用途、處理方式等信息。生態(tài)環(huán)境部門(mén)會(huì)依據(jù)相關(guān)環(huán)保法規(guī),評(píng)估試劑進(jìn)口對(duì)環(huán)境的潛在影響,如是否符合污染物排放標(biāo)準(zhǔn)、是否具備妥善的廢棄物處理方案等。只有在獲得環(huán)保部門(mén)許可后,企業(yè)才能進(jìn)行后續(xù)進(jìn)口操作,確保生物試劑進(jìn)口不會(huì)對(duì)國(guó)內(nèi)生態(tài)環(huán)境造成危害。涉及人類(lèi)遺傳資源的生物試劑進(jìn)口,受《中華人民共和國(guó)人類(lèi)遺傳資源管理?xiàng)l例》約束。進(jìn)口單位必須向有關(guān)部門(mén)科學(xué)技術(shù)行政部門(mén)申請(qǐng)人類(lèi)遺傳資源許可。申請(qǐng)過(guò)程中,需詳細(xì)說(shuō)明試劑來(lái)源、涉及的人類(lèi)遺傳資源種類(lèi)與數(shù)量、使用目的、合作方信息等。有關(guān)部...
2025-04-24 -
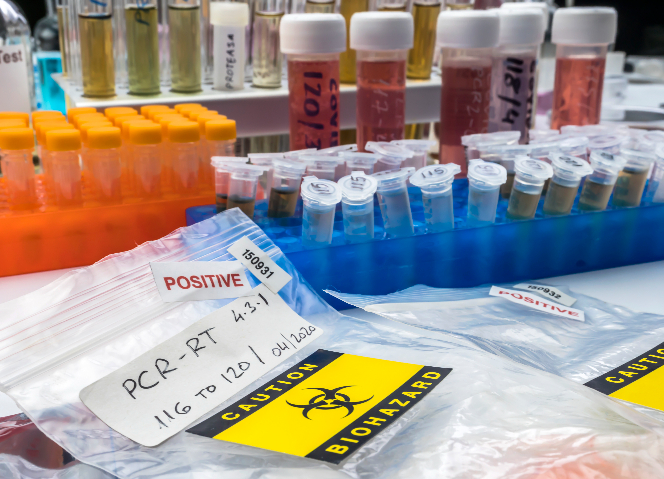 杭州抗體試劑進(jìn)出口報(bào)關(guān)
杭州抗體試劑進(jìn)出口報(bào)關(guān)進(jìn)出口生物試劑均需通過(guò)嚴(yán)格檢驗(yàn)檢疫。出口時(shí),企業(yè)要主動(dòng)向海關(guān)與檢驗(yàn)檢疫部門(mén)申報(bào),提供詳細(xì)產(chǎn)品信息、生產(chǎn)批次、質(zhì)量檢測(cè)報(bào)告等資料。檢驗(yàn)檢疫部門(mén)會(huì)根據(jù)試劑特性與進(jìn)口國(guó)要求,進(jìn)行質(zhì)量抽檢,檢測(cè)純度、活性、微生物限度等指標(biāo),對(duì)于一些傳染病診斷試劑,對(duì)其微生物限度和特異性要求極高。對(duì)可能攜帶病原體、有害生物因子的試劑進(jìn)行生物安全檢測(cè),防止有害生物跨境傳播。進(jìn)口生物試劑時(shí),同樣要接受我國(guó)檢驗(yàn)檢疫部門(mén)查驗(yàn),企業(yè)需配合做好貨物查驗(yàn)、抽樣檢測(cè)等工作,對(duì)于冷鏈生物試劑,還要滿(mǎn)足冷鏈貨物檢驗(yàn)檢疫要求,如落實(shí)核酸檢測(cè)、消毒等防控措施,確保產(chǎn)品符合國(guó)內(nèi)外檢驗(yàn)檢疫標(biāo)準(zhǔn),保障公共衛(wèi)生安全與市場(chǎng)秩序,為國(guó)內(nèi)科研、醫(yī)療等領(lǐng)域提...
2025-04-24 -
 上海港細(xì)胞培養(yǎng)試劑進(jìn)出口審批流程
上海港細(xì)胞培養(yǎng)試劑進(jìn)出口審批流程對(duì)于特殊生物制品類(lèi)生物試劑,如疫苗類(lèi)、血液制品類(lèi)及血源篩查用診斷試劑等,進(jìn)口審批更為嚴(yán)格。進(jìn)口企業(yè)必須提前向國(guó)家藥品監(jiān)督管理局申請(qǐng)進(jìn)口批件。申請(qǐng)時(shí),需提供產(chǎn)品的詳細(xì)信息,包括生產(chǎn)工藝、質(zhì)量標(biāo)準(zhǔn)、穩(wěn)定性研究數(shù)據(jù)、臨床使用情況等資料,以證明產(chǎn)品質(zhì)量可靠、安全有效且符合國(guó)內(nèi)需求。國(guó)家藥品監(jiān)督管理局會(huì)組織人員對(duì)申請(qǐng)資料進(jìn)行多方面審評(píng),只有在獲得進(jìn)口批件后,企業(yè)才具備此類(lèi)生物試劑的進(jìn)口資格,防止不合格或高風(fēng)險(xiǎn)特殊生物制品流入國(guó)內(nèi)。生物試劑進(jìn)口需關(guān)注目的國(guó)對(duì)生物試劑銷(xiāo)售渠道的限制。上海港細(xì)胞培養(yǎng)試劑進(jìn)出口審批流程進(jìn)出口生物試劑都要經(jīng)過(guò)嚴(yán)格檢驗(yàn)檢疫。出口時(shí),企業(yè)要主動(dòng)向海關(guān)與檢驗(yàn)檢疫部門(mén)申報(bào),提供詳細(xì)的產(chǎn)品...
2025-04-24 -
 昆山生物試劑出口審批單
昆山生物試劑出口審批單技術(shù)創(chuàng)新是生物試劑進(jìn)出口發(fā)展的重心驅(qū)動(dòng)力。在研發(fā)環(huán)節(jié),基因編輯技術(shù)如 CRISPR-Cas9 的突破,催生了一系列新型基因編輯生物試劑,這些試劑在科研和基因醫(yī)療領(lǐng)域需求大增,推動(dòng)了相關(guān)試劑的進(jìn)出口。例如,國(guó)外先進(jìn)企業(yè)研發(fā)的高精細(xì) CRISPR 基因編輯試劑盒,憑借技術(shù)優(yōu)勢(shì)易售全球,國(guó)內(nèi)企業(yè)也積極引進(jìn)并進(jìn)行本地化生產(chǎn)與改進(jìn),促進(jìn)了該類(lèi)試劑的進(jìn)出口貿(mào)易。納米技術(shù)應(yīng)用于生物試劑,開(kāi)發(fā)出納米級(jí)診斷試劑、藥物載體試劑等,提升了試劑性能,拓展了應(yīng)用范圍,打開(kāi)了新的市場(chǎng)需求。此外,生物信息學(xué)技術(shù)助力生物試劑研發(fā)數(shù)據(jù)處理與分析,加速新型試劑研發(fā)進(jìn)程,研發(fā)成果轉(zhuǎn)化為產(chǎn)品后推動(dòng)生物試劑進(jìn)出口業(yè)務(wù)邁向更高技術(shù)水平,...
2025-04-24 -
 蘇州抗體試劑進(jìn)出口貿(mào)易
蘇州抗體試劑進(jìn)出口貿(mào)易生物試劑進(jìn)口前,產(chǎn)品注冊(cè)是關(guān)鍵環(huán)節(jié)。按藥品管理的生物試劑,需向 NMPA 提交注冊(cè)申請(qǐng),包含產(chǎn)品研發(fā)、生產(chǎn)工藝、質(zhì)量標(biāo)準(zhǔn)、臨床試驗(yàn)數(shù)據(jù)(如適用)等詳細(xì)資料,經(jīng)嚴(yán)格審評(píng)審批流程,審評(píng)中心評(píng)估產(chǎn)品安全性、有效性和質(zhì)量可控性,審批通過(guò)后方可獲得進(jìn)口藥品注冊(cè)證。醫(yī)療器械類(lèi)生物試劑注冊(cè)同樣嚴(yán)謹(jǐn),依據(jù)風(fēng)險(xiǎn)程度分為不同類(lèi)別管理。低風(fēng)險(xiǎn)產(chǎn)品實(shí)行備案管理,進(jìn)口商向所在地設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門(mén)提交備案資料;中、高風(fēng)險(xiǎn)產(chǎn)品則需向 NMPA 申請(qǐng)注冊(cè),經(jīng)技術(shù)審評(píng)、臨床試驗(yàn)核查(若有)等程序,取得醫(yī)療器械注冊(cè)證后才能進(jìn)口,確保進(jìn)口產(chǎn)品符合國(guó)內(nèi)質(zhì)量與安全要求。生物試劑進(jìn)口需嚴(yán)格遵守目的國(guó)的生物安全相關(guān)管理規(guī)定。蘇州抗...
2025-04-23 -
 昆山特殊物品進(jìn)口流程
昆山特殊物品進(jìn)口流程進(jìn)出口生物試劑均需通過(guò)嚴(yán)格檢驗(yàn)檢疫。出口時(shí),企業(yè)要主動(dòng)向海關(guān)與檢驗(yàn)檢疫部門(mén)申報(bào),提供詳細(xì)產(chǎn)品信息、生產(chǎn)批次、質(zhì)量檢測(cè)報(bào)告等資料。檢驗(yàn)檢疫部門(mén)會(huì)根據(jù)試劑特性與進(jìn)口國(guó)要求,進(jìn)行質(zhì)量抽檢,檢測(cè)純度、活性、微生物限度等指標(biāo),對(duì)于一些傳染病診斷試劑,對(duì)其微生物限度和特異性要求極高。對(duì)可能攜帶病原體、有害生物因子的試劑進(jìn)行生物安全檢測(cè),防止有害生物跨境傳播。進(jìn)口生物試劑時(shí),同樣要接受我國(guó)檢驗(yàn)檢疫部門(mén)查驗(yàn),企業(yè)需配合做好貨物查驗(yàn)、抽樣檢測(cè)等工作,對(duì)于冷鏈生物試劑,還要滿(mǎn)足冷鏈貨物檢驗(yàn)檢疫要求,如落實(shí)核酸檢測(cè)、消毒等防控措施,確保產(chǎn)品符合國(guó)內(nèi)外檢驗(yàn)檢疫標(biāo)準(zhǔn),保障公共衛(wèi)生安全與市場(chǎng)秩序,為國(guó)內(nèi)科研、醫(yī)療等領(lǐng)域提...
2025-04-23 -
 特殊物品進(jìn)口政策
特殊物品進(jìn)口政策包裝對(duì)于生物試劑進(jìn)出口至關(guān)重要。從材質(zhì)選擇上,要依據(jù)試劑特性而定。例如,強(qiáng)酸強(qiáng)堿類(lèi)化學(xué)試劑生物試劑,需采用耐酸堿腐蝕的玻璃或特殊塑料材質(zhì)包裝,防止包裝被腐蝕而導(dǎo)致試劑泄漏。對(duì)于有遮光要求的試劑,像某些光敏性生物活性試劑,包裝需使用棕色玻璃或添加遮光材料的包裝容器,避免光照引發(fā)試劑變質(zhì)。在包裝結(jié)構(gòu)方面,要確保密封性良好,對(duì)于易揮發(fā)或需隔絕空氣的試劑,會(huì)采用多層密封包裝,并可能添加干燥劑、脫氧劑等輔助材料。同時(shí),包裝外部要有清晰、準(zhǔn)確的標(biāo)識(shí),標(biāo)注試劑名稱(chēng)、規(guī)格、儲(chǔ)存條件、危險(xiǎn)警示等信息,且標(biāo)識(shí)要符合國(guó)際通用標(biāo)準(zhǔn)以及目標(biāo)市場(chǎng)的法規(guī)要求,以保障運(yùn)輸、儲(chǔ)存和使用過(guò)程中的安全與便利。生物試劑進(jìn)口過(guò)程中,需...
2025-04-23 -
 上海核酸試劑進(jìn)出口免費(fèi)咨詢(xún)
上海核酸試劑進(jìn)出口免費(fèi)咨詢(xún)若生物試劑含有毒有害物質(zhì),進(jìn)口前需通過(guò)環(huán)保部門(mén)的審批。企業(yè)要向當(dāng)?shù)厣鷳B(tài)環(huán)境部門(mén)提交進(jìn)口申請(qǐng),說(shuō)明生物試劑所含毒有害物質(zhì)的種類(lèi)、含量、用途、處理方式等信息。生態(tài)環(huán)境部門(mén)會(huì)依據(jù)相關(guān)環(huán)保法規(guī),評(píng)估試劑進(jìn)口對(duì)環(huán)境的潛在影響,如是否符合污染物排放標(biāo)準(zhǔn)、是否具備妥善的廢棄物處理方案等。只有在獲得環(huán)保部門(mén)許可后,企業(yè)才能進(jìn)行后續(xù)進(jìn)口操作,確保生物試劑進(jìn)口不會(huì)對(duì)國(guó)內(nèi)生態(tài)環(huán)境造成危害。涉及人類(lèi)遺傳資源的生物試劑進(jìn)口,受《中華人民共和國(guó)人類(lèi)遺傳資源管理?xiàng)l例》約束。進(jìn)口單位必須向有關(guān)部門(mén)科學(xué)技術(shù)行政部門(mén)申請(qǐng)人類(lèi)遺傳資源許可。申請(qǐng)過(guò)程中,需詳細(xì)說(shuō)明試劑來(lái)源、涉及的人類(lèi)遺傳資源種類(lèi)與數(shù)量、使用目的、合作方信息等。有關(guān)部...
2025-04-23 -
 南京核酸試劑進(jìn)出口審批單
南京核酸試劑進(jìn)出口審批單生物試劑進(jìn)口前,產(chǎn)品注冊(cè)是關(guān)鍵環(huán)節(jié)。按藥品管理的生物試劑,需向 NMPA 提交注冊(cè)申請(qǐng),包含產(chǎn)品研發(fā)、生產(chǎn)工藝、質(zhì)量標(biāo)準(zhǔn)、臨床試驗(yàn)數(shù)據(jù)(如適用)等詳細(xì)資料,經(jīng)嚴(yán)格審評(píng)審批流程,審評(píng)中心評(píng)估產(chǎn)品安全性、有效性和質(zhì)量可控性,審批通過(guò)后方可獲得進(jìn)口藥品注冊(cè)證。醫(yī)療器械類(lèi)生物試劑注冊(cè)同樣嚴(yán)謹(jǐn),依據(jù)風(fēng)險(xiǎn)程度分為不同類(lèi)別管理。低風(fēng)險(xiǎn)產(chǎn)品實(shí)行備案管理,進(jìn)口商向所在地設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門(mén)提交備案資料;中、高風(fēng)險(xiǎn)產(chǎn)品則需向 NMPA 申請(qǐng)注冊(cè),經(jīng)技術(shù)審評(píng)、臨床試驗(yàn)核查(若有)等程序,取得醫(yī)療器械注冊(cè)證后才能進(jìn)口,確保進(jìn)口產(chǎn)品符合國(guó)內(nèi)質(zhì)量與安全要求。對(duì)于生物試劑出口,需向進(jìn)口國(guó)提供詳細(xì)的產(chǎn)品技術(shù)資料。南京核...
2025-04-23 -
 杭州免疫診斷試劑進(jìn)出口許可證辦理
杭州免疫診斷試劑進(jìn)出口許可證辦理生物試劑進(jìn)口的標(biāo)簽與說(shuō)明書(shū)必須符合國(guó)內(nèi)政策要求。標(biāo)簽應(yīng)清晰標(biāo)注產(chǎn)品名稱(chēng)、規(guī)格、生產(chǎn)企業(yè)、生產(chǎn)日期、有效期、儲(chǔ)存條件、批準(zhǔn)文號(hào)(注冊(cè)證編號(hào))等關(guān)鍵信息,且文字表述應(yīng)準(zhǔn)確、規(guī)范,使用中文(可同時(shí)標(biāo)注外文)。說(shuō)明書(shū)內(nèi)容要詳盡,涵蓋產(chǎn)品組成、適用范圍、使用方法、注意事項(xiàng)、不良反應(yīng)等信息,為使用者提供多方面指導(dǎo)。對(duì)于診斷類(lèi)生物試劑,說(shuō)明書(shū)還需明確檢測(cè)原理、性能指標(biāo)、臨床預(yù)期用途等內(nèi)容。標(biāo)簽與說(shuō)明書(shū)的格式和內(nèi)容需經(jīng)監(jiān)管部門(mén)審核,確保其符合《藥品說(shuō)明書(shū)和標(biāo)簽管理規(guī)定》《醫(yī)療器械說(shuō)明書(shū)和標(biāo)簽管理規(guī)定》等法規(guī),避免誤導(dǎo)使用者,保障患者和消費(fèi)者權(quán)益。對(duì)于生物試劑出口,要提前掌握進(jìn)口國(guó)的檢疫程序。杭州免疫診斷試劑進(jìn)...
2025-04-23 -
 上海酶類(lèi)試劑進(jìn)出口前置審批備案
上海酶類(lèi)試劑進(jìn)出口前置審批備案出口生物試劑的企業(yè)需滿(mǎn)足多方面資質(zhì)條件。首先,企業(yè)要完成對(duì)外貿(mào)易經(jīng)營(yíng)者備案登記,具備合法出口經(jīng)營(yíng)權(quán)。若生產(chǎn)出口藥品類(lèi)生物試劑,必須持有有效的藥品生產(chǎn)許可證,且生產(chǎn)車(chē)間符合 GMP 要求,保證產(chǎn)品質(zhì)量穩(wěn)定可靠。對(duì)于醫(yī)療器械類(lèi)生物試劑出口,企業(yè)需依據(jù)產(chǎn)品風(fēng)險(xiǎn)等級(jí),持有相應(yīng)的醫(yī)療器械生產(chǎn)許可證或完成生產(chǎn)備案。此外,企業(yè)應(yīng)建立完善的質(zhì)量管理體系,配備熟悉出口法規(guī)、產(chǎn)品技術(shù)以及國(guó)際市場(chǎng)規(guī)則的專(zhuān)業(yè)團(tuán)隊(duì),以確保出口業(yè)務(wù)順利開(kāi)展并符合各國(guó)監(jiān)管要求。生物試劑進(jìn)口需關(guān)注目的國(guó)對(duì)生物試劑使用人群的限定。上海酶類(lèi)試劑進(jìn)出口前置審批備案在生物試劑進(jìn)出口領(lǐng)域,法規(guī)政策起著關(guān)鍵的規(guī)范作用。不同國(guó)家和地區(qū)對(duì)生物試劑的進(jìn)出口有...
2025-04-23 -
 蘇州生物試劑出口前置審批備案
蘇州生物試劑出口前置審批備案技術(shù)創(chuàng)新是生物試劑進(jìn)出口發(fā)展的重心驅(qū)動(dòng)力。在研發(fā)環(huán)節(jié),基因編輯技術(shù)如 CRISPR-Cas9 的突破,催生了一系列新型基因編輯生物試劑,這些試劑在科研和基因醫(yī)療領(lǐng)域需求大增,推動(dòng)了相關(guān)試劑的進(jìn)出口。例如,國(guó)外先進(jìn)企業(yè)研發(fā)的高精細(xì) CRISPR 基因編輯試劑盒,憑借技術(shù)優(yōu)勢(shì)易售全球,國(guó)內(nèi)企業(yè)也積極引進(jìn)并進(jìn)行本地化生產(chǎn)與改進(jìn),促進(jìn)了該類(lèi)試劑的進(jìn)出口貿(mào)易。納米技術(shù)應(yīng)用于生物試劑,開(kāi)發(fā)出納米級(jí)診斷試劑、藥物載體試劑等,提升了試劑性能,拓展了應(yīng)用范圍,打開(kāi)了新的市場(chǎng)需求。此外,生物信息學(xué)技術(shù)助力生物試劑研發(fā)數(shù)據(jù)處理與分析,加速新型試劑研發(fā)進(jìn)程,研發(fā)成果轉(zhuǎn)化為產(chǎn)品后推動(dòng)生物試劑進(jìn)出口業(yè)務(wù)邁向更高技術(shù)水平,...
2025-04-23 -
 寧波酶類(lèi)試劑進(jìn)出口
寧波酶類(lèi)試劑進(jìn)出口生物試劑對(duì)運(yùn)輸條件要求嚴(yán)苛。多數(shù)生物試劑具有溫度敏感性,像酶、抗體等,運(yùn)輸中需嚴(yán)格維持特定溫度范圍,否則易失活。常用冷鏈運(yùn)輸方式,包括干冰冷藏(適用于少量試劑短途運(yùn)輸,但要注意干冰揮發(fā)安全問(wèn)題,確保包裝通風(fēng))、低溫冷藏車(chē)(適合大量試劑長(zhǎng)距離運(yùn)輸,車(chē)內(nèi)制冷設(shè)備需精細(xì)控溫)以及專(zhuān)業(yè)冷鏈物流服務(wù)。企業(yè)要挑選具備專(zhuān)業(yè)資質(zhì)和豐富經(jīng)驗(yàn)的運(yùn)輸商,運(yùn)輸前仔細(xì)檢查設(shè)備運(yùn)行狀況,運(yùn)輸中實(shí)時(shí)監(jiān)控溫度并做好記錄,保證溫度符合試劑儲(chǔ)存要求。對(duì)于易氧化、潮解或需惰性氣體保護(hù)的生物試劑,要采用適配的包裝和防護(hù)措施,防止試劑變質(zhì)。出口生物試劑選擇物流時(shí),要考慮其在進(jìn)口國(guó)的清關(guān)能力。寧波酶類(lèi)試劑進(jìn)出口生物試劑出口需通過(guò)嚴(yán)格的檢...
2025-04-23 -
 杭州生物試劑進(jìn)口貿(mào)易
杭州生物試劑進(jìn)口貿(mào)易藥品類(lèi)生物試劑進(jìn)口需依據(jù)《藥品進(jìn)口管理辦法》進(jìn)行備案。進(jìn)口單位必須向經(jīng)有關(guān)部門(mén)批準(zhǔn)的 18 個(gè)指定口岸城市(如北京、上海、廣州等)的口岸藥品監(jiān)督管理局提出進(jìn)口備案申請(qǐng)。進(jìn)口時(shí),需提交《進(jìn)口藥品報(bào)驗(yàn)單》、裝箱單、提運(yùn)單、發(fā)票、《進(jìn)口藥品注冊(cè)證》(或者《醫(yī)藥產(chǎn)品注冊(cè)證》)復(fù)印件、《進(jìn)口藥品批件》復(fù)印件等資料。若進(jìn)口單位為經(jīng)營(yíng)企業(yè),還應(yīng)提供《藥品經(jīng)營(yíng)許可證》復(fù)印件。口岸藥品監(jiān)督管理局在收到完備資料后,對(duì)符合要求的申請(qǐng),會(huì)在規(guī)定時(shí)間內(nèi)簽發(fā)《進(jìn)口藥品通關(guān)單》,作為海關(guān)驗(yàn)放藥品的重要依據(jù),確保藥品類(lèi)生物試劑合法合規(guī)進(jìn)入國(guó)內(nèi)市場(chǎng)。出口生物試劑要重視進(jìn)口國(guó)對(duì)標(biāo)簽內(nèi)容完整性的要求。杭州生物試劑進(jìn)口貿(mào)易生物試劑出...
2025-04-22 -
 無(wú)錫生物試劑進(jìn)出口前置審批備案
無(wú)錫生物試劑進(jìn)出口前置審批備案質(zhì)量管控貫穿生物試劑進(jìn)出口全程。生產(chǎn)環(huán)節(jié),出口企業(yè)要遵循嚴(yán)格質(zhì)量標(biāo)準(zhǔn),如國(guó)際標(biāo)準(zhǔn)化組織(ISO)相關(guān)質(zhì)量管理體系要求,從原材料采購(gòu)開(kāi)始把控,確保其符合純度、活性等指標(biāo)。生產(chǎn)過(guò)程在符合 GMP 的潔凈車(chē)間進(jìn)行,防止微生物污染。產(chǎn)品出廠前經(jīng)過(guò)多輪質(zhì)量檢測(cè),包括物理性質(zhì)、化學(xué)組成、生物活性測(cè)定等。進(jìn)口企業(yè)在接收貨物時(shí),也需進(jìn)行嚴(yán)格驗(yàn)收,對(duì)照合同與質(zhì)量標(biāo)準(zhǔn),檢查試劑外觀、包裝完整性,抽樣進(jìn)行質(zhì)量復(fù)核。若發(fā)現(xiàn)質(zhì)量問(wèn)題,及時(shí)與供應(yīng)商溝通協(xié)商退換貨。海關(guān)在查驗(yàn)時(shí),對(duì)生物試劑質(zhì)量也會(huì)抽檢,確保進(jìn)口產(chǎn)品符合我國(guó)質(zhì)量要求,保障國(guó)內(nèi)科研、醫(yī)療等領(lǐng)域使用安全。出口生物試劑選擇物流時(shí),要評(píng)估其在途跟蹤服務(wù)。無(wú)錫生物試劑...
2025-04-22 -
 杭州生物試劑進(jìn)出口前置審批備案
杭州生物試劑進(jìn)出口前置審批備案生物試劑對(duì)運(yùn)輸條件要求嚴(yán)苛。多數(shù)生物試劑具有溫度敏感性,像酶、抗體等,運(yùn)輸中需嚴(yán)格維持特定溫度范圍,否則易失活。常用冷鏈運(yùn)輸方式,包括干冰冷藏(適用于少量試劑短途運(yùn)輸,但要注意干冰揮發(fā)安全問(wèn)題,確保包裝通風(fēng))、低溫冷藏車(chē)(適合大量試劑長(zhǎng)距離運(yùn)輸,車(chē)內(nèi)制冷設(shè)備需精細(xì)控溫)以及專(zhuān)業(yè)冷鏈物流服務(wù)。企業(yè)要挑選具備專(zhuān)業(yè)資質(zhì)和豐富經(jīng)驗(yàn)的運(yùn)輸商,運(yùn)輸前仔細(xì)檢查設(shè)備運(yùn)行狀況,運(yùn)輸中實(shí)時(shí)監(jiān)控溫度并做好記錄,保證溫度符合試劑儲(chǔ)存要求。對(duì)于易氧化、潮解或需惰性氣體保護(hù)的生物試劑,要采用適配的包裝和防護(hù)措施,防止試劑變質(zhì)。出口生物試劑選擇物流時(shí),要考量其與進(jìn)口國(guó)當(dāng)?shù)嘏渌偷你暯印:贾萆镌噭┻M(jìn)出口前置審批備案生物試劑進(jìn)...
2025-04-22 -
 上海生物試劑出口政策
上海生物試劑出口政策生物試劑進(jìn)出口業(yè)務(wù)與可持續(xù)發(fā)展緊密相連。從生產(chǎn)角度,企業(yè)越來(lái)越注重綠色生產(chǎn)工藝,采用環(huán)保型原材料和節(jié)能生產(chǎn)設(shè)備,減少生產(chǎn)過(guò)程中的能源消耗和污染物排放。例如,一些生物試劑生產(chǎn)企業(yè)優(yōu)化發(fā)酵工藝,提高原料利用率,降低廢水廢氣產(chǎn)生量。在包裝方面,推行可回收、可降解包裝材料,減少塑料等一次性包裝的使用,像紙質(zhì)包裝逐漸替代部分塑料包裝用于生物試劑運(yùn)輸。在運(yùn)輸環(huán)節(jié),運(yùn)輸企業(yè)采用優(yōu)化的物流路線(xiàn)規(guī)劃,提高運(yùn)輸效率,降低能源消耗。同時(shí),國(guó)際上也在推動(dòng)生物試劑進(jìn)出口行業(yè)的可持續(xù)發(fā)展標(biāo)準(zhǔn)制定,促使企業(yè)在追求經(jīng)濟(jì)效益的同時(shí),積極履行社會(huì)責(zé)任,實(shí)現(xiàn)行業(yè)的長(zhǎng)期可持續(xù)發(fā)展。生物試劑進(jìn)口申報(bào)時(shí),需明確試劑的生物活性等級(jí)。上海生...
2025-04-22 -
 酶類(lèi)試劑進(jìn)出口前置審批代辦
酶類(lèi)試劑進(jìn)出口前置審批代辦生物試劑進(jìn)口前,產(chǎn)品注冊(cè)是關(guān)鍵環(huán)節(jié)。按藥品管理的生物試劑,需向 NMPA 提交注冊(cè)申請(qǐng),包含產(chǎn)品研發(fā)、生產(chǎn)工藝、質(zhì)量標(biāo)準(zhǔn)、臨床試驗(yàn)數(shù)據(jù)(如適用)等詳細(xì)資料,經(jīng)嚴(yán)格審評(píng)審批流程,審評(píng)中心評(píng)估產(chǎn)品安全性、有效性和質(zhì)量可控性,審批通過(guò)后方可獲得進(jìn)口藥品注冊(cè)證。醫(yī)療器械類(lèi)生物試劑注冊(cè)同樣嚴(yán)謹(jǐn),依據(jù)風(fēng)險(xiǎn)程度分為不同類(lèi)別管理。低風(fēng)險(xiǎn)產(chǎn)品實(shí)行備案管理,進(jìn)口商向所在地設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門(mén)提交備案資料;中、高風(fēng)險(xiǎn)產(chǎn)品則需向 NMPA 申請(qǐng)注冊(cè),經(jīng)技術(shù)審評(píng)、臨床試驗(yàn)核查(若有)等程序,取得醫(yī)療器械注冊(cè)證后才能進(jìn)口,確保進(jìn)口產(chǎn)品符合國(guó)內(nèi)質(zhì)量與安全要求。生物試劑進(jìn)口需關(guān)注目的國(guó)對(duì)生物試劑銷(xiāo)售渠道的限制。酶類(lèi)試劑...
2025-04-22 -
 上海港生物試劑進(jìn)口前置審批代辦
上海港生物試劑進(jìn)口前置審批代辦生物試劑進(jìn)出口企業(yè)必須滿(mǎn)足嚴(yán)格資質(zhì)要求。在國(guó)內(nèi),從事生物試劑進(jìn)出口的企業(yè)首先要具備合法的進(jìn)出口經(jīng)營(yíng)權(quán),需在商務(wù)部門(mén)完成對(duì)外貿(mào)易經(jīng)營(yíng)者備案登記。若涉及藥品類(lèi)生物試劑進(jìn)出口,企業(yè)必須取得藥品經(jīng)營(yíng)許可證,且其倉(cāng)儲(chǔ)、運(yùn)輸?shù)葪l件要符合藥品經(jīng)營(yíng)質(zhì)量管理規(guī)范(GSP)。對(duì)于醫(yī)療器械類(lèi)生物試劑,企業(yè)需進(jìn)行醫(yī)療器械經(jīng)營(yíng)備案或取得醫(yī)療器械經(jīng)營(yíng)許可證,依據(jù)試劑風(fēng)險(xiǎn)等級(jí)而定。企業(yè)的人員資質(zhì)也至關(guān)重要,要有熟悉生物試劑法規(guī)、質(zhì)量控制和進(jìn)出口業(yè)務(wù)流程的專(zhuān)業(yè)人員,如質(zhì)量管理人員需具備相關(guān)專(zhuān)業(yè)背景及從業(yè)經(jīng)驗(yàn)。此外,企業(yè)還需通過(guò)海關(guān)的信用評(píng)級(jí),良好的信用等級(jí)有助于加快貨物通關(guān)速度,保障進(jìn)出口業(yè)務(wù)高效運(yùn)行。生物試劑進(jìn)口需關(guān)注目的...
2025-04-22 -
 南京抗體試劑進(jìn)出口前置審批備案
南京抗體試劑進(jìn)出口前置審批備案特殊生物試劑進(jìn)口有著更為嚴(yán)苛的政策。高風(fēng)險(xiǎn)生物制品類(lèi)試劑,如某些用于血液篩查的診斷試劑,除滿(mǎn)足常規(guī)進(jìn)口要求外,還需依據(jù)《生物制品批簽發(fā)管理辦法》,在進(jìn)口前取得生物制品批簽發(fā)證明,確保每批次產(chǎn)品質(zhì)量安全。涉及人類(lèi)遺傳資源的生物試劑進(jìn)口,受《中華人民共和國(guó)人類(lèi)遺傳資源管理?xiàng)l例》監(jiān)管,進(jìn)口單位需提前申請(qǐng)人類(lèi)遺傳資源許可,防止我國(guó)人類(lèi)遺傳資源非法外流,同時(shí)保證試劑用于合法科研、醫(yī)療等用途。此外,對(duì)于含有毒有害物質(zhì)或受管控生物因子的生物試劑,需符合環(huán)保、生物安全等多部門(mén)聯(lián)合制定的進(jìn)口政策,履行相應(yīng)審批與監(jiān)管流程。生物試劑進(jìn)口過(guò)程中,要防范因政策變動(dòng)導(dǎo)致的風(fēng)險(xiǎn)。南京抗體試劑進(jìn)出口前置審批備案我國(guó)生物試劑出...
2025-04-22 -
 上海細(xì)胞培養(yǎng)試劑進(jìn)出口檢驗(yàn)檢疫
上海細(xì)胞培養(yǎng)試劑進(jìn)出口檢驗(yàn)檢疫生物試劑進(jìn)出口領(lǐng)域存在多種國(guó)際合作模式。一種是跨國(guó)企業(yè)間的聯(lián)合研發(fā)合作,例如歐美藥企與亞洲生物試劑企業(yè)合作,利用歐美企業(yè)的研發(fā)資金和技術(shù)優(yōu)勢(shì),結(jié)合亞洲企業(yè)的人力成本與市場(chǎng)資源,共同開(kāi)發(fā)新型生物試劑,研發(fā)成果通過(guò)雙方進(jìn)出口渠道推向全球市場(chǎng)。另一種是技術(shù)授權(quán)合作模式,擁有先進(jìn)生物試劑技術(shù)的企業(yè)將技術(shù)授權(quán)給其他國(guó)家企業(yè),被授權(quán)企業(yè)負(fù)責(zé)本地化生產(chǎn)與銷(xiāo)售,技術(shù)授權(quán)方則通過(guò)收取授權(quán)費(fèi)和銷(xiāo)售分成獲利,促進(jìn)生物試劑技術(shù)在國(guó)際間流動(dòng)與產(chǎn)品進(jìn)出口。還有產(chǎn)業(yè)園區(qū)合作模式,不同國(guó)家共建生物產(chǎn)業(yè)園區(qū),園區(qū)內(nèi)企業(yè)共享資源、技術(shù)和市場(chǎng),在生物試劑進(jìn)出口方面形成產(chǎn)業(yè)集群優(yōu)勢(shì),提升整體國(guó)際競(jìng)爭(zhēng)力,推動(dòng)生物試劑進(jìn)出口業(yè)務(wù)協(xié)同發(fā)展...
2025-04-22 -
 杭州抗體試劑進(jìn)出口許可證辦理
杭州抗體試劑進(jìn)出口許可證辦理進(jìn)出口生物試劑,契合目標(biāo)市場(chǎng)標(biāo)準(zhǔn)是關(guān)鍵。出口時(shí),產(chǎn)品必須滿(mǎn)足進(jìn)口國(guó)法規(guī)及相關(guān)國(guó)際標(biāo)準(zhǔn)。例如出口歐盟,生物試劑需符合歐盟指令與協(xié)調(diào)標(biāo)準(zhǔn),通過(guò) CE 認(rèn)證,涵蓋安全性、健康影響等多方面評(píng)估;出口美國(guó),則要符合美國(guó)食品藥品監(jiān)督管理局(FDA)要求并完成對(duì)應(yīng)注冊(cè)程序。進(jìn)口生物試劑時(shí),要確保符合我國(guó)藥品、醫(yī)療器械等相關(guān)法規(guī)。藥品類(lèi)生物試劑需符合我國(guó)藥品注冊(cè)標(biāo)準(zhǔn),從成分純度到穩(wěn)定性都有明確規(guī)范;醫(yī)療器械類(lèi)生物試劑要完成國(guó)內(nèi)注冊(cè)或備案,產(chǎn)品研發(fā)、生產(chǎn)、質(zhì)量控制等各環(huán)節(jié)都得達(dá)標(biāo),否則無(wú)法順利通關(guān),更不能進(jìn)入市場(chǎng)銷(xiāo)售,甚至可能面臨召回與處罰。生物試劑進(jìn)口需關(guān)注目的國(guó)對(duì)實(shí)驗(yàn)室用試劑的管理辦法。杭州抗體試劑進(jìn)出口許...
2025-04-22 -
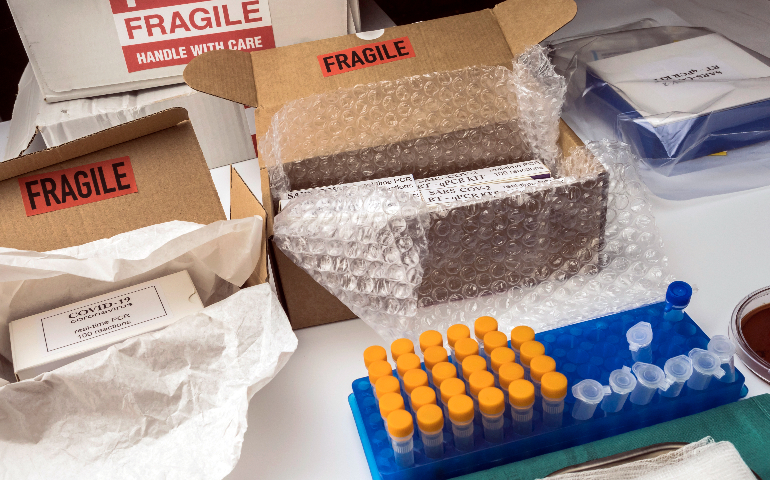 昆山抗體試劑進(jìn)出口監(jiān)管法規(guī)
昆山抗體試劑進(jìn)出口監(jiān)管法規(guī)包裝對(duì)于生物試劑進(jìn)出口至關(guān)重要。從材質(zhì)選擇上,要依據(jù)試劑特性而定。例如,強(qiáng)酸強(qiáng)堿類(lèi)化學(xué)試劑生物試劑,需采用耐酸堿腐蝕的玻璃或特殊塑料材質(zhì)包裝,防止包裝被腐蝕而導(dǎo)致試劑泄漏。對(duì)于有遮光要求的試劑,像某些光敏性生物活性試劑,包裝需使用棕色玻璃或添加遮光材料的包裝容器,避免光照引發(fā)試劑變質(zhì)。在包裝結(jié)構(gòu)方面,要確保密封性良好,對(duì)于易揮發(fā)或需隔絕空氣的試劑,會(huì)采用多層密封包裝,并可能添加干燥劑、脫氧劑等輔助材料。同時(shí),包裝外部要有清晰、準(zhǔn)確的標(biāo)識(shí),標(biāo)注試劑名稱(chēng)、規(guī)格、儲(chǔ)存條件、危險(xiǎn)警示等信息,且標(biāo)識(shí)要符合國(guó)際通用標(biāo)準(zhǔn)以及目標(biāo)市場(chǎng)的法規(guī)要求,以保障運(yùn)輸、儲(chǔ)存和使用過(guò)程中的安全與便利。生物試劑進(jìn)口需遵循目的...
2025-04-22 -
 上海生物試劑進(jìn)口審批單代辦
上海生物試劑進(jìn)口審批單代辦進(jìn)出口生物試劑,契合目標(biāo)市場(chǎng)標(biāo)準(zhǔn)是關(guān)鍵。出口時(shí),產(chǎn)品必須滿(mǎn)足進(jìn)口國(guó)法規(guī)及相關(guān)國(guó)際標(biāo)準(zhǔn)。例如出口歐盟,生物試劑需符合歐盟指令與協(xié)調(diào)標(biāo)準(zhǔn),通過(guò) CE 認(rèn)證,涵蓋安全性、健康影響等多方面評(píng)估;出口美國(guó),則要符合美國(guó)食品藥品監(jiān)督管理局(FDA)要求并完成對(duì)應(yīng)注冊(cè)程序。進(jìn)口生物試劑時(shí),要確保符合我國(guó)藥品、醫(yī)療器械等相關(guān)法規(guī)。藥品類(lèi)生物試劑需符合我國(guó)藥品注冊(cè)標(biāo)準(zhǔn),從成分純度到穩(wěn)定性都有明確規(guī)范;醫(yī)療器械類(lèi)生物試劑要完成國(guó)內(nèi)注冊(cè)或備案,產(chǎn)品研發(fā)、生產(chǎn)、質(zhì)量控制等各環(huán)節(jié)都得達(dá)標(biāo),否則無(wú)法順利通關(guān),更不能進(jìn)入市場(chǎng)銷(xiāo)售,甚至可能面臨召回與處罰。生物試劑進(jìn)口需關(guān)注目的國(guó)對(duì)生物試劑使用人群的限定。上海生物試劑進(jìn)口審批...
2025-04-22 -
 蘇州細(xì)胞培養(yǎng)試劑進(jìn)出口審批代辦
蘇州細(xì)胞培養(yǎng)試劑進(jìn)出口審批代辦在生物試劑進(jìn)出口過(guò)程中,完善的文件管理和記錄保存不可或缺。企業(yè)要妥善保存各類(lèi)進(jìn)出口相關(guān)文件,包括合同,詳細(xì)記錄雙方權(quán)利義務(wù);發(fā)票,明確交易金額等關(guān)鍵信息;裝箱單,說(shuō)明貨物包裝明細(xì);提單,作為貨物所有權(quán)憑證;報(bào)關(guān)單,記錄貨物進(jìn)出口申報(bào)信息;檢驗(yàn)檢疫報(bào)告,證明產(chǎn)品質(zhì)量合規(guī);資質(zhì)證書(shū),展示企業(yè)經(jīng)營(yíng)資格;認(rèn)證文件,體現(xiàn)產(chǎn)品符合特定標(biāo)準(zhǔn)等。這些文件不是通關(guān)必備,也是企業(yè)日后追溯業(yè)務(wù)流程、應(yīng)對(duì)監(jiān)管檢查的重要依據(jù)。同時(shí),企業(yè)內(nèi)部要建立詳細(xì)記錄制度,記錄試劑從采購(gòu)(生產(chǎn))、運(yùn)輸、儲(chǔ)存到銷(xiāo)售(出口)各環(huán)節(jié)信息,如溫度記錄,監(jiān)控運(yùn)輸儲(chǔ)存過(guò)程中的溫度變化;質(zhì)量檢測(cè)結(jié)果,及時(shí)掌握產(chǎn)品質(zhì)量狀況;操作流程,規(guī)范員工操作行...
2025-04-22 -
 無(wú)錫生物試劑進(jìn)出口審批單代辦
無(wú)錫生物試劑進(jìn)出口審批單代辦醫(yī)療器械類(lèi)生物試劑進(jìn)口前,需依據(jù)風(fēng)險(xiǎn)等級(jí)完成注冊(cè)審批。低風(fēng)險(xiǎn)的一類(lèi)醫(yī)療器械生物試劑,進(jìn)口商需向所在地設(shè)區(qū)的市級(jí)藥品監(jiān)督管理部門(mén)辦理備案手續(xù),提交產(chǎn)品風(fēng)險(xiǎn)分析資料、產(chǎn)品技術(shù)要求、產(chǎn)品檢驗(yàn)報(bào)告等備案資料。對(duì)于中風(fēng)險(xiǎn)的二類(lèi)和高風(fēng)險(xiǎn)的三類(lèi)醫(yī)療器械生物試劑,則要向國(guó)家藥品監(jiān)督管理局申請(qǐng)注冊(cè)。企業(yè)需準(zhǔn)備詳細(xì)的產(chǎn)品研發(fā)、生產(chǎn)制造、臨床評(píng)價(jià)等資料,經(jīng)技術(shù)審評(píng)、臨床試驗(yàn)核查(如適用)等嚴(yán)格程序,獲得醫(yī)療器械注冊(cè)證后,方可開(kāi)展進(jìn)口業(yè)務(wù),保障進(jìn)口醫(yī)療器械類(lèi)生物試劑的安全性與有效性。生物試劑進(jìn)口要了解目的國(guó)海關(guān)對(duì)其查驗(yàn)的重點(diǎn)與流程。無(wú)錫生物試劑進(jìn)出口審批單代辦生物試劑進(jìn)口前,產(chǎn)品注冊(cè)是關(guān)鍵環(huán)節(jié)。按藥品管理的生物試劑,...
2025-04-21